Was ist Reinstoff?
Reinstoffe sind chemische Substanzen mit einer einheitlichen Zusammensetzung und klar definierten physikalischen und chemischen Eigenschaften. Diese Stoffe bestehen aus nur einer Art von Teilchen, seien es Atome oder Moleküle. Im Unterschied zu Gemischen wie Luft oder Salzwasser enthalten Reinstoffe keine Beimischungen anderer Substanzen. Bekannte Beispiele im Alltag umfassen Elemente wie Wasserstoff, Sauerstoff und Kohlenstoff sowie Verbindungen wie Natriumchlorid (Kochsalz) und destilliertes Wasser.
Der Begriff „Reinstoff“ umfasst sowohl einfache Elemente als auch komplexere chemische Verbindungen. Solche Stoffe besitzen stets konstante Merkmale, wie Schmelz- und Siedepunkte, die unabhängig vom Ursprungsort des Materials bleiben. Diese spezielle Kategorie der Stoffe zeichnet sich durch ihre besondere Homogenität aus, was sie ideal für Anwendungen in Wissenschaft und Industrie macht. Beispielsweise wird reines Eisen in metallurgischen Prozessen verwendet, während reines Gold und Silber nicht nur für Schmuck, sondern auch in der Elektronik unverzichtbar sind.
Das Wichtigste in Kürze
- Reinstoffe bestehen aus nur einer Art von Teilchen: Atomen oder Molekülen.
- Sie haben konstante physikalische und chemische Eigenschaften, wie spezifische Schmelz- und Siedepunkte.
- Reinstoffe umfassen Elemente (z.B. Wasserstoff) und Verbindungen (z.B. Natriumchlorid).
- Unterscheidung zu Gemischen: Reinstoffe sind homogen, während Gemische unterschiedliche Zusammensetzungen haben.
- Anwendungen: genutzt in der Industrie, Wissenschaft und täglichen Leben (z.B. destilliertes Wasser, reines Eisen).
In der Chemie sind Reinstoffe Substanzen, die aus nur einer Art von chemischen Element oder Verbindung bestehen. Diese Substanzen können nicht weiter in andere Substanzen durch physikalische Methoden wie Filtration oder Destillation unterteilt werden. Beispiele für Reinstoffe sind Elemente wie Gold oder Sauerstoff sowie Verbindungen wie Wasser (H2O) oder Kochsalz (NaCl).
Reinstoff Definition Chemie und Eigenschaften
Reinstoffe sind chemische Substanzen, die aus nur einer Art von Teilchen bestehen und keine Verunreinigungen enthalten. Diese Teilchen können entweder Atome oder Moleküle sein. Ein charakteristisches Merkmal von Reinstoffen ist ihre einheitliche Zusammensetzung, was bedeutet, dass die chemischen Eigenschaften über das gesamte Material hinweg konstant bleiben.
Ein klassisches Beispiel für einen Reinstoff ist ein Element wie Wasserstoff, Sauerstoff oder Kohlenstoff. Elemente bestehen aus nur einer Art von Atom. Ebenso gibt es Verbindungen, die ebenfalls als Reinstoffe betrachtet werden, wenn sie keine anderen Stoffe enthalten. Beispiele hierfür sind Natriumchlorid (Kochsalz) und Methan.
Zu den spezifischen Eigenschaften von Reinstoffen zählen ihr definierter Schmelzpunkt und Siedepunkt. Das heißt, sie schmelzen und sieden bei genau festgelegten Temperaturen. Dies ermöglicht es, Reinstoffe durch physikalische Methoden zu identifizieren und von Gemischen zu unterscheiden. So hat beispielsweise destilliertes Wasser eine sehm hohe Reinheit und besitzt genau definierte thermodynamische Eigenschaften.
Zusätzlich zeigen Reinstoffe keinerlei Trennung in verschiedene Phasen unter normalen Bedingungen. Ob in einem festen Zustand wie Reines Eisen oder Reines Silber, in flüssiger Form wie Wasser oder im gasförmigen Zustand wie Methan – die Partikel bleiben homogen verteilt.
Ein weiteres Beispiel aus der Anwendung ist Reines Gold. In seiner reinen Form ist Gold nicht nur kostbar, sondern auch äußerst widerstandsfähig gegen Korrosion.
Die Chemie handelt von Stoffen und den Veränderungen, denen sie unterliegen. – Marie Curie
| Beispiel für Reinstoff | Eigenschaften |
|---|---|
| Wasserstoff | Leichtestes Element, farbloses Gas |
| Sauerstoff | Unentbehrlich für die Atmung, farbloses Gas |
| Kohlenstoff | Grundbestandteil organischer Verbindungen, feste Form |
| Natriumchlorid | Essentiell in der Küche, weiße Kristalle |
| Destilliertes Wasser | Reinheit von 99,9%, keine Mineralien |
| Methan | Hauptbestandteil von Erdgas, farbloses Gas |
| Reines Eisen | Stark und formbar, metallisches Element |
| Reines Gold | Höchste Reinheit, gelb schimmerndes Metall |
| Reines Silber | Strahlend weißes Metall, hohe Leitfähigkeit |
Unterschiede zwischen Reinstoffen und Gemischen
Reinstoffe und Gemische unterscheiden sich grundlegend in ihrer Zusammensetzung und ihren Eigenschaften. Ein Reinstoff besteht aus nur einem einzigen chemischen Element oder einer chemischen Verbindung, während ein Gemisch aus zwei oder mehr verschiedenen Stoffen zusammengesetzt ist.
Bei Reinstoffen bleiben die physikalischen und chemischen Eigenschaften konstant. Das bedeutet, dass Wasserstoff, Sauerstoff und Kohlenstoff jeweils ihre eigenen spezifischen Merkmale aufweisen, egal wie viel man von ihnen hat. Im Gegensatz dazu variieren die Eigenschaften eines Gemisches je nach den enthaltenen Stoffen und deren Verhältnissen zueinander. Zum Beispiel zeigt eine Mischung aus Wasser und Salz je nach Konzentration unterschiedliche physikalische Eigenschaften wie Siedepunkt und Dichte.
Ein weiterer Unterschied liegt im Trennungsverfahren. Bei Reinstoffen sind solche Verfahren nicht notwendig, da keine fremden Substanzen vorhanden sind. Hingegen erfordert das Trennen eines Gemisches in seine Bestandteile spezielle Methoden wie Filtration, Destillation oder Chromatographie. So kann beispielsweise destilliertes Wasser durch Destillation vom gewöhnlichen Leitungswasser abgetrennt werden, um alle Verunreinigungen zu entfernen.
Zusätzlich bleibt die chemische Struktur von Reinstoffen unverändert, solange sie rein bleiben. Reines Eisen, reines Gold und reines Silber behalten immer ihre molekularen Strukturen bei, unabhängig von der Menge oder Form. In einem Gemisch hingegen können chemische Reaktionen zwischen den Komponenten stattfinden, wodurch neue Verbindungen entstehen können.
Daher spielen Reinstoffe eine wichtige Rolle in der Chemie und Technik, da sie klare und vorhersehbare Eigenschaften bieten, während Gemische oft komplexere Verhaltensmuster zeigen.
Beispiele für Reinstoffe im Alltag
Im Alltag begegnen uns viele Reinstoffe, auch wenn wir es oft nicht bemerken. Ein klassisches Beispiel ist destilliertes Wasser, das durch seine Reinheit ideale Bedingungen für Laborarbeiten schafft und auch in medizinischen Anwendungen genutzt wird. H2O (Wasser) ist ein Reinstoff. Wasser besteht aus nur einer Art von chemischer Verbindung, die aus zwei Wasserstoffatomen und einem Sauerstoffatom besteht. Daher wird Wasser als Reinstoff betrachtet.
Ein weiteres weit verbreitetes Beispiel ist Natriumchlorid, besser bekannt als Kochsalz. Dieses Molekül besteht nur aus Natrium- und Chlorionen und ist in der Küche unverzichtbar. Auch Sauerstoff, ein lebensnotwendiges Gas, kommt in reiner Form in Sauerstoffflaschen zur medizinischen Versorgung zum Einsatz.
In der Schmuckherstellung und bei elektrischen Leitungen spielt reines Gold eine wichtige Rolle. Es zeichnet sich durch seine ausgezeichnete Leitfähigkeit und Korrosionsbeständigkeit aus.
Wer an Brennstoffe denkt, kommt auf Methan, das als Hauptbestandteil von Erdgas gilt. In seinem reinen Zustand weist Methan eine hohe Energiedichte auf und ist wichtig für die Energieversorgung. Aber auch reines Silber findet in hochwertigen elektronischen Bauteilen Anwendung wegen seiner hervorragenden elektrischen Eigenschaften.
Hausbesitzer nutzen reines Eisen in verschiedenen Konstruktionen und Werkzeugen aufgrund seiner Festigkeit und Haltbarkeit. Schließlich sind Elemente wie Wasserstoff und Kohlenstoff fundamental in vielen Prozessen und Produkten, sei es in der Chemieindustrie oder bei modernen Energietechnologien.
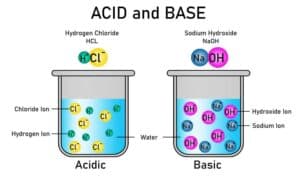
Salze sind auch Reinstoffe in der Chemie. Salze bestehen aus positiv geladenen Metallionen und negativ geladenen Nichtmetallionen, die sich durch ionische Bindungen miteinander verbinden. Beispiele für Salze sind Natriumchlorid (NaCl), Kaliumnitrat (KNO3) und Calciumcarbonat (CaCO3). Salze sind wichtige chemische Verbindungen und spielen eine entscheidende Rolle in vielen chemischen Reaktionen und in biologischen Prozessen.
Methoden zur Identifikation von Reinstoffen
Um Reinstoffe zu identifizieren, werden verschiedene Methoden eingesetzt. Eine wesentliche Methode ist die Massenspektrometrie, bei der die Masse von Atomen oder Molekülen sehr präzise gemessen wird. Dies ermöglicht es, Elemente wie Wasserstoff, Sauerstoff und Kohlenstoff zuverlässig zu erkennen.
Ein weiteres Verfahren ist die Infrarotspektroskopie. Hierbei wird das Absorptionsspektrum eines Stoffes im Infrarotbereich analysiert. Jede Verbindung hat ein einzigartiges Spektrum, was es erlaubt, Verbindungen wie Natriumchlorid oder Methan eindeutig zu bestimmen.
Die Röntgendiffraktometrie ist außerdem eine wichtige Technik zur Identifizierung kristalliner Reinstoffe, einschließlich Reines Eisen und Reines Gold. Diese Methode nutzt die Beugung von Röntgenstrahlen an Kristallen, um die atomare Struktur zu ermitteln.
Zusätzlich können chemische Eigenschaften analysiert werden. Zum Beispiel zeigt Distilliertes Wasser als Reinstoff genau definierte Schmelz- und Siedepunkte, die sich von denen von Gemischen unterscheiden lassen.
Mit diesen und anderen Analysen kann man auch die Reinheit von Substanzen feststellen. So beinhalten beispielsweise Reines Silber oder andere Metalle häufig geringe Mengen von Verunreinigungen, wodurch Spezialverfahren notwendig sind, um deren Echtheit nachzuweisen.
Diese Methoden zusammen ermöglichen es Wissenschaftlern und Ingenieuren, hochwertige und zuverlässige Materialien für vielfältige Anwendungen bereitzustellen.
Anwendung von Reinstoffen in der Industrie
In der Industrie spielen Reinstoffe eine entscheidende Rolle, da sie garantieren, dass chemische Prozesse mit höchster Präzision und Effizienz ablaufen. Beispielsweise wird reines Eisen in der Metallverarbeitung verwendet, um hochfeste Stähle zu erzeugen, die in Bauprojekten oder Fahrzeuganwendungen zum Einsatz kommen.
Ein weiteres Beispiel ist distilliertes Wasser, das in Laboratorien und verschiedenen Herstellungsprozessen als Lösungsmittel dient, da es frei von Verunreinigungen ist und somit keine unerwünschten Nebenreaktionen verursacht. In der Pharmazie werden hochreine Chemikalien benötigt, um Medikamente herzustellen, deren Wirksamkeit und Sicherheit garantiert sein müssen.
Auch Edelmetalle wie reines Gold und reines Silber finden in der Elektronikindustrie Verwendung. Diese Metalle werden aufgrund ihrer hohen Leitfähigkeit und Korrosionsbeständigkeit für die Herstellung von Kontakten, Leiterplatten und anderen Bauteilen genutzt. Reines Natriumchlorid wird häufig in der Lebensmittelindustrie eingesetzt, da es als Speisesalz unverzichtbar ist.
In der Petrochemie spielt Methan als wichtiger Rohstoff für die Herstellung von Kunststoffen eine Rolle. Darüber hinaus wird Methan auch zur Energiegewinnung verwendet.
| Reinstoff | Symbol | Verwendung |
|---|---|---|
| Wasserstoff | H | Kraftstoff, chemische Synthese |
| Sauerstoff | O | Atmung, industrielle Oxidation |
| Kohlenstoff | C | Grundstoff der Organik, Werkstoffe |
| Natriumchlorid | NaCl | Lebensmittel, Streusalz |
| Destilliertes Wasser | H2O | Labor, Medizin |
| Methan | CH4 | Energieträger, chemische Industrie |
| Reines Eisen | Fe | Bauindustrie, Werkzeugherstellung |
| Reines Gold | Au | Schmuck, Elektronik |
| Reines Silber | Ag | Elektronik, Schmuck |
Vorteile und Nachteile von Reinstoffen
Reinstoffe bieten viele Vorteile, insbesondere in der Wirtschaft und im Bereich der Wissenschaft. Da sie aus nur einer Art von Teilchen bestehen, sei es ein Element oder eine Verbindung, ermöglichen sie genaue und zuverlässige Ergebnisse bei Experimenten und technischen Anwendungen. Zum Beispiel kann reines Eisen in der Metallverarbeitung für spezielle Legierungen verwendet werden, während destilliertes Wasser in Laboratorien unerlässlich ist, da es frei von Verunreinigungen ist.
Ein weiterer Vorteil von Reinstoffen liegt in ihrer voraussagbaren und konsistenten Eigenschaften. Dies ist entscheidend in Bereichen wie Pharmazie und Nahrungsmittelherstellung, wo bestimmte Standards eingehalten werden müssen, um die Qualität und Sicherheit zu gewährleisten. Beispielsweise wird Natriumchlorid (Kochsalz) sowohl in der Medizin als auch in Haushalten genutzt, sofern seine Reinheit gesichert ist.
Allerdings gibt es auch Nachteile. Die Herstellung und Reinigung von Reinstoffen können sehr aufwendig und kostenintensiv sein. Der Prozess, reines Silber oder reines Gold zu gewinnen, erfordert spezialisierte Techniken und Technologien, was sich im Preis dieser Materialien widerspiegelt.
Ein weiteres Problem liegt in der möglichen Reaktivität einiger Reinstoffe. Elemente wie Wasserstoff und Sauerstoff sind hochreaktiv und erfordern besondere Sicherheitsmaßnahmen beim Umgang. Ebenso kann Methan, obwohl es ein sauberer Brennstoff ist, explosive Risiken bergen, wenn es nicht sorgfältig gehandhabt wird.
Zusammengefasst haben Reinstoffe signifikante positive Aspekte, aber auch einige Herausforderungen bezüglich Kosten und Sicherheit, die bedacht werden sollten.
Chemische Herstellung und Reinigungsverfahren
Die chemische Herstellung und Reinigung von Reinstoffen erfordert präzise Verfahren, um Verunreinigungen zu entfernen und die gewünschte Reinheit zu erreichen. Diese Prozesse sind besonders in der Industrie von großer Bedeutung, um hochwertige Materialien zu erzeugen.
Eines der häufig genutzten Verfahren zur Erzeugung von Reinstoffen ist die Destillation. Hierbei wird eine Flüssigkeit durch Erhitzen zum Sieden gebracht und anschließend das Dampfprodukt kondensiert, sodass man einen reinen Stoff erhält. Ein klassisches Beispiel im Alltag ist destilliertes Wasser, das frei von gelösten Salzen und Mineralien ist.
Ein weiteres wichtiges Reinigungsverfahren ist die Kristallisation. Bei diesem Prozess werden Stoffe in einer Lösung aufgelöst und beim langsamen Abkühlen kristallisieren sie als reine Substanzen aus. Dies findet Anwendung bei der Aufbereitung von reinen Elementen wie Sauerstoff, Kohlenstoff oder reinem Eisen.
In der Elektrolyse wird elektrische Energie genutzt, um chemische Verbindungen in ihre Bestandteile zu zerlegen. Dadurch kann man Metalle wie reines Gold und reines Silber herstellen, die in vielen technologischen Anwendungen benötigt werden.
Für gasförmige Reinstoffe wird oft die Gasseparierung eingesetzt. Beispielsweise erfolgt die Gewinnung von reinem Wasserstoff durch Zerlegung von Methan oder anderen kohlenwasserstoffhaltigen Gasen.
Zusammengefasst lassen sich durch sorgfältig angewandte chemische Herstellungs- und Reinigungsverfahren hochreine Stoffe erhalten, die für zahlreiche wissenschaftliche und industrielle Anwendungen unerlässlich sind.
Historische Entwicklung und Entdeckung von Reinstoffen
Die Entdeckung von Reinstoffen geht auf die Anfänge der Chemie zurück. Schon im antiken Griechenland untersuchten Philosophen wie Demokrit und Aristoteles die Natur von Materie, ohne jedoch die modernen Konzepte der Elemente zu kennen. Erst im 17. Jahrhundert legte der Chemiker Robert Boyle den Grundstein für das moderne Verständnis von Elementen und Verbindungen.
Im 18. Jahrhundert entdeckte Antoine Lavoisier die Rolle des Sauerstoffs in chemischen Reaktionen und widerlegte damit frühere Theorien. Seine Arbeiten trugen wesentlich zur Definition von Elementen als grundlegende Bausteine der Materie bei. Ein bekanntes Beispiel aus dieser Zeit ist die Trennung von Wasser durch Elektrolyse, wobei reiner Wasserstoff und Sauerstoff nachgewiesen wurden.
Mit dem Fortschreiten der Wissenschaft entdeckten Chemiker immer mehr Reinstoffe. Der britische Forscher Humphry Davy isolierte im frühen 19. Jahrhundert erstmals Natrium und Kalium durch Elektrolyse geschmolzener Salze. Später folgten andere bedeutende Entdeckungen wie reines Eisen und reines Gold, was die Liste der bekannten Reinstoffe weiter erweiterte.
Bis ins späte 19. und frühe 20. Jahrhundert führte die Verbesserung analytischer Techniken, wie Spektroskopie und Chromatographie, zu einer genaueren Identifikation und Charakterisierung von Reinstoffen. Heute sind diese Technologien unverzichtbar für die Forschung und Industrieanwendung von Stoffen wie Methan, reines Silber und destilliertes Wasser.