Was sind Isomere?
Isomere sind chemische Verbindungen, die trotz derselben Summenformel unterschiedliche Strukturen und Eigenschaften aufweisen. Diese Vielfalt resultiert aus der unterschiedlichen Anordnung von Atomen innerhalb eines Moleküls. In der Chemie werden Isomere in zwei Hauptkategorien unterteilt: Strukturisomere und Stereoisomere. Strukturisomere, auch als Konstitutionsisomere bekannt, unterscheiden sich in der Ketten- oder Skelettstruktur ihrer Atome.
Stereoisomere hingegen haben dieselbe Konnektivität zwischen den Atomen, aber ihre räumliche Anordnung variiert. Unter den Stereoisomeren gibt es Enantiomere und Diastereomere. Während Enantiomere durch Chiralität charakterisiert sind und ein asymmetrisches Zentrum besitzen, unterscheiden sich Diastereomere nicht nur in ihren internen Winkeln und Bindungslängen, sondern auch in anderen physikalischen und chemischen Eigenschaften.
Die Analyse und Identifikation von Isomeren erfordert spezielle Methoden, darunter Kristallstrukturanalysen und NMR-Spektroskopie. Durch das Verständnis der verschiedenen Typen und Eigenschaften von Isomeren können Chemiker Einblicke in Reaktionsmechanismen und molekulare Wechselwirkungen gewinnen.
Das Wichtigste in Kürze
- Isomere haben gleiche Summenformel, aber unterschiedliche Strukturen und Eigenschaften.
- Es gibt Strukturisomere und Stereoisomere, beide mit eigenen Unterkategorien.
- Strukturisomere unterscheiden sich in der Anordnung der Atombindungen.
- Stereoisomere unterscheiden sich in der räumlichen Anordnung der Atome.
- NMR-Spektroskopie und HPLC sind wichtige Methoden zur Isomerenanalyse.
Isomere sind Moleküle, die dieselbe chemische Formel haben, aber sich in der Anordnung der Atome im Molekül unterscheiden. Sie besitzen also unterschiedliche Strukturen, was zu verschiedenen chemischen und physikalischen Eigenschaften führen kann. Isomere können in verschiedene Kategorien unterteilt werden, wie Strukturisomere, Stereoisomere und Konstitutionsisomere, je nach Art der strukturellen Unterschiede. Das Konzept der Isomerie ist wichtig, um die Vielfalt der chemischen Verbindungen und ihre unterschiedlichen Verhaltensweisen zu verstehen.
Definition von Isomeren
Isomere sind chemische Verbindungen, die dieselbe Summenformel haben, aber unterschiedliche Strukturen. Diese unterschiedlichen Strukturen führen dazu, dass Isomere oft verschiedene physikalische und chemische Eigenschaften aufweisen.
Grundsätzlich werden Isomere in zwei Hauptkategorien unterteilt: Strukturisomere und Stereoisomere. Strukturisomere, auch als Konstitutionsisomere bekannt, unterscheiden sich in der Anordnung ihrer Atome und chemischen Bindungen. Dies bedeutet, dass die Reihenfolge, in der die Atome aneinander gebunden sind, verschieden ist, was zu unterschiedlichen Molekülstrukturen führt.
Auf der anderen Seite stehen die Stereoisomere, bei denen die gleiche Anordnung von Bindungen vorliegt, die jedoch eine unterschiedliche räumliche Anordnung der Atome und Gruppen zeigen. Stereoisomere können weiter in zwei Untergruppen unterteilt werden: Diastereomere und Enantiomere. Diastereomere unterscheiden sich nicht spiegelbildlich voneinander, während Enantiomere spiegelbildliche Isomere sind und eine besondere Relevanz in der Chiralität und asymmetrischen Zentren haben.
Diese Unterschiede in der Raumerfüllung und Atomanordnung beeinflussen maßgeblich die chemischen Eigenschaften und Reaktionsmechanismen der Isomere. Beispielsweise kann ein Strukturisomer aufgrund seiner Kristallstruktur andere Schmelzpunkte oder Siedepunkte haben als ein anderes Isomer derselben Verbindung. Die Identifikation und Analyse von Isomeren, etwa durch Methoden wie die NMR-Spektroskopie, spielt daher eine wichtige Rolle in der organischen Chemie.
Die Chemie des Lebens ist die Chemie der Isomere. – Linus Pauling
Beispiele für Isomere in der Chemie sind:
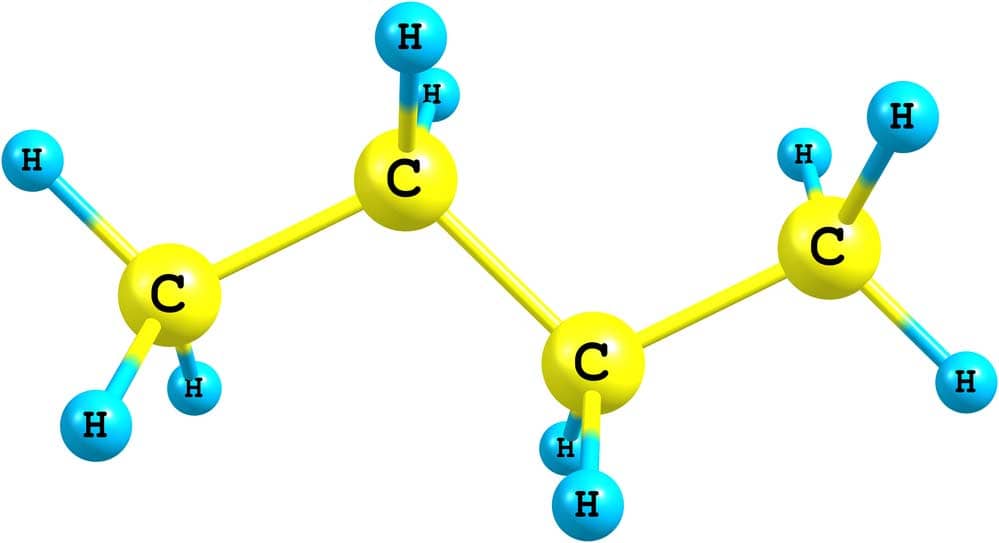
- Butan und Isobutan: Beide haben die chemische Formel C₄H₁₀, aber unterschiedliche Strukturen.
- Glucose und Fruktose: Beide haben die chemische Formel C₆H₁₂O₆, aber unterschiedliche Strukturen und Eigenschaften.
- Ethen und Propen: Beide haben die chemische Formel C₂H₄, aber unterschiedliche Strukturen und chemische Eigenschaften.
- Essigsäureethylester und Methylethylketon: Beide haben die gleiche Summenformel C₄H₈O, aber unterschiedliche Strukturen und chemische Eigenschaften.
Arten
Es gibt verschiedene Arten von Isomeren in der Chemie. Hier sind einige davon:
- Strukturisomere: Isomere, die sich in der Anordnung der Atome unterscheiden, z.B. Kettenisomere und Positionsisomere.
- Stereoisomere: Isomere, die sich in der räumlichen Anordnung der Atome unterscheiden, z.B. E-Z-Isomere und Diastereomer.
- Konstitutionsisomere: Isomere, die sich in der Reihenfolge, in der die Atome miteinander verbunden sind, unterscheiden, z.B. Kettenisomere und Funktionsisomere.
Diese verschiedenen Arten von Isomeren zeigen die Vielfalt der Strukturvariationen, die in chemischen Verbindungen auftreten können. Es gibt auch noch Unterarten, wie diese zum Beipiel:
Stellungsisomere sind eine Art von Strukturisomeren. Stellungsisomere sind Isomere, die sich in der Position funktioneller Gruppen innerhalb des Moleküls unterscheiden. Diese Isomere haben die gleiche Molekülformel, aber die funktionellen Gruppen sind an unterschiedlichen Positionen im Molekül angeordnet. Stellungsisomere sind ein Beispiel für die Vielfalt der Strukturisomere in der organischen Chemie.
Enantiomere sind ebenfalls eine Art von Stereoisomeren in der Chemie. Enantiomere sind spiegelbildliche Isomere, die sich nur in ihrer räumlichen Anordnung unterscheiden. Sie sind nicht überlagerbar und haben die gleiche chemische und physikalische Eigenschaften, abgesehen von ihrer Reaktion mit anderen chiralen Molekülen oder polarisiertem Licht. Enantiomere spielen eine wichtige Rolle in der Chemie, insbesondere in der pharmazeutischen Industrie und der Biochemie.
Diastereomere sind eine weitere Art von Stereoisomeren in der Chemie. Diastereomere sind Isomere, die sich in ihrer räumlichen Anordnung unterscheiden, aber nicht spiegelbildlich zueinander sind. Im Gegensatz zu Enantiomeren haben Diastereomere unterschiedliche chemische und physikalische Eigenschaften und können sich in ihren Reaktionen verhalten. Diastereomere entstehen, wenn Moleküle mehr als eine Chiralitätszentrum haben oder wenn sie unterschiedliche Konfigurationen um ein oder mehrere Chiralitätszentren aufweisen.
Auch die Cis-Trans-Isomerie ist eine Form der Stereoisomerie in der Chemie. Bei der Cis-Trans-Isomerie handelt es sich um eine spezielle Art von Stereoisomerie, bei der sich Moleküle aufgrund der relativen Position von Substituenten um eine Doppelbindung unterscheiden. In cis-Isomeren befinden sich die Substituenten auf derselben Seite der Doppelbindung, während sie in trans-Isomeren sich auf gegenüberliegenden Seiten der Doppelbindung befinden. Diese Art von Isomerie ist häufig bei Verbindungen mit Doppelbindungen wie Alkenen und Cycloalkenen anzutreffen.
Neben den bereits erwähnten Arten von Isomeren gibt es noch weitere Unterarten in der Chemie, wie zum Beispiel:
- Konformationsisomere: Isomere, die aufgrund der Rotation um Einfachbindungen unterschiedliche räumliche Konformationen aufweisen.
- Tautomere: Isomere, die sich durch eine Wanderung von Wasserstoffatomen und Doppelbindungen im Molekül unterscheiden, z.B. Keto-Enol-Tautomerie.
- Ringisomere: Isomere, die sich in der Ringstruktur eines Moleküls unterscheiden, z.B. bei cyclischen Verbindungen.
Diese verschiedenen Unterarten von Isomeren zeigen die Vielfalt der strukturellen Variationen und Beziehungen zwischen chemischen Verbindungen in der Chemie.
| Isomer-Typ | Beschreibung |
|---|---|
| Konstitutionsisomere | Unterschiedliche Reihenfolge der Atombindungen, was zu verschiedenen Molekülstrukturen führt. |
| Enantiomere | Spiegelbildlich zueinander, besitzen ein asymmetrisches Zentrum, wichtig in der Chiralität. |
| Diastereomere | Stereoisomere, die nicht spiegelbildlich zueinander sind, unterscheiden sich in physikalischen und chemischen Eigenschaften. |
| Cis-Trans-Isomerie | Eine Form der Diastereomerie, die sich in der Position von Substituenten um eine Doppelbindung oder Ringstruktur unterscheidet. |
Strukturisomere vs Stereoisomere
In der organischen Chemie gibt es zwei Haupttypen von Isomeren: Strukturisomere und Stereoisomere. Strukturisomere, auch bekannt als Konstitutionsisomere, haben die gleiche chemische Formel, aber eine unterschiedliche Anordnung ihrer Atome. Das bedeutet, dass ihre Funktionellen Gruppen und chemischen Bindungen unterschiedlich angeordnet sind. Ein klassisches Beispiel hierfür sind Butan und Isobutan (C4H10), die zwar dieselbe Molekülformel besitzen, sich aber in ihrer Struktur und damit in ihren Eigenschaften grundlegend unterscheiden.
Stereoisomere hingegen behalten sowohl die gleiche molekulare Formel als auch die gleiche Reihenfolge der Atomanordnung bei, doch sie unterscheiden sich in der räumlichen Orientierung ihrer Atome. Zu den Stereoisomeren gehören Enantiomere und Diastereomere. Enantiomere sind Spiegelbilder voneinander und haben oft sehr unterschiedliche chemische Eigenschaften, insbesondere in Bezug auf Reaktionsmechanismen mit anderen chiralitätsabhängigen Molekülen, während Diastereomere keine Spiegelbilder sind und ebenfalls verschiedene physikalische und chemische Eigenschaften aufweisen können.
Die Unterschiede zwischen Strukturisomeren und Stereoisomeren spielen eine entscheidende Rolle bei der Bestimmung der Molekülstruktur und beeinflussen stark die Eigenschaften und das Verhalten von organischen Verbindungen. Durch Techniken wie NMR-Spektroskopie lassen sich diese Unterschiede analysieren und identifizieren. Diese Unterscheidung ist besonders wichtig in der Pharmakologie, wo selbst kleine Abweichungen in der Molekularstruktur oder -symmetrie drastische Auswirkungen auf die Wirksamkeit und Sicherheit eines Medikaments haben können.
Cis-Trans-Isomerie in Alkenen
Cis-Trans-Isomerie ist eine Form der Stereoisomerie, die bei Alkenen auftritt. Bei dieser Isomerie handelt es sich um die unterschiedliche räumliche Anordnung von Substituenten an den Kohlenstoffatomen einer Doppelbindung. Diese besondere Konfiguration führt zu unterschiedlichen physikalischen und chemischen Eigenschaften der Isomere.
Betrachtet man ein Alken mit zwei gleichen Substituenten an beiden Seiten der Doppelbindung, können diese entweder auf derselben Seite (cis) oder auf gegenüberliegenden Seiten (trans) liegen. Zum Beispiel hat das Molekül 2-Buten zwei solche Formen: cis-2-Buten und trans-2-Buten. Im cis-Isomer sind die Methylgruppen auf derselben Seite der Doppelbindung angeordnet, während sie im trans-Isomer auf gegenüberliegenden Seiten liegen.
Diese Unterschiede in der Atomanordnung führen zu Variationen in der Kristallstruktur, was wiederum verschiedene Schmelz- und Siedepunkte zur Folge hat. Cis-Isomere neigen dazu, niedrigere Schmelzpunkte zu haben als Trans-Isomere, da die Krümmung der Moleküle weniger dichtes Packen ermöglicht. Auf der anderen Seite haben Trans-Isomere oft höhere Schmelzpunkte und größere thermische Stabilität aufgrund ihrer symmetrischeren Struktur.
Die Untersuchung der cis-trans-Isomerie spielt eine wichtige Rolle bei der Analyse von Verbindungen mittels Techniken wie NMR-Spektroskopie. Eine korrekte Unterscheidung und Charakterisierung kann direkt auf verschiedene biologische und chemische Reaktionsmechanismen Einfluss nehmen, vor allem in der organischen Chemie und der Pharmakologie, wo die richtigen Aktionswege für Medikamente bestimmt werden müssen.
Enantiomere und chirale Moleküle
Enantiomere sind eine spezielle Art von Isomeren, die in der organischen Chemie besonders relevant sind. Diese Verbindungen weisen Chiralität auf, das heißt, sie besitzen ein asymmetrisches Zentrum und existieren daher als zwei spiegelbildliche Formen zueinander. Diese Formen werden häufig als „rechtsdrehend“ (R) und „linksdrehend“ (S) bezeichnet.
Ein typisches Merkmal chiraler Moleküle ist, dass ihre Enantiomere dieselbe chemische Zusammensetzung und ähnliche physikalische Eigenschaften besitzen. Dennoch besitzen sie völlig unterschiedliche biologische Aktivitäten. Dies liegt daran, dass viele biologische Systeme ebenfalls chiral sind und somit unterschiedlich auf die Enantiomere reagieren. Ein Beispiel hierfür sind Medikamente, bei denen ein Enantiomer mehr erwünschte Wirkungen zeigt, während das andere möglicherweise weniger effektiv oder sogar schädlich sein kann.
Die Asymmetrie im Molekül spielt hierbei eine entscheidende Rolle. Chiralität kommt oft durch die Anwesenheit eines Kohlenstoffatoms zustande, welches vier verschiedene Substituenten trägt. Diese einzigartige Anordnung führt dazu, dass die beiden Enantiomere nicht zur Deckung gebracht werden können, ähnlich wie unsere linken und rechten Hände.
Durch verschiedene Methoden wie NMR-Spektroskopie oder chromatographische Techniken lassen sich Enantiomere voneinander trennen und analysieren. Die gezielte Untersuchung der Enantiomere und ihrer Wirkung hat große Bedeutung für pharmazeutische Anwendungen und ermöglicht die Entwicklung spezifischer Arzneimittel mit verbesserter Wirksamkeit und Sicherheit.
Eigenschaften und Anwendung von Isomeren
Isomere besitzen unterschiedliche chemische und physikalische Eigenschaften, obwohl sie die gleiche molekulare Formel haben. Diese Unterschiede ergeben sich aus der spezifischen Anordnung ihrer Atome und den daraus resultierenden Strukturen. Zum Beispiel können Strukturisomere wie Konstitutionsisomere verschiedene Siedepunkte, Schmelzpunkte oder Dichten aufweisen, abhängig von ihrer Molekülstruktur.
Stereoisomere, einschließlich Diastereomere und Enantiomere, unterscheiden sich in der räumlichen Anordnung ihrer Atome. Ein chiralitätsbedingter Unterschied bei Enantiomeren führt dazu, dass sie unterschiedliche optische Aktivitäten zeigen – das heißt, sie drehen polarisiertes Licht in entgegengesetzte Richtungen. Dies ist besonders relevant in der Pharmakologie, da oft nur ein Enantiomer einer Verbindung die gewünschte biologische Aktivität besitzt, während das andere wirkungslos oder sogar schädlich sein kann.
Chiralität und asymmetrische Zentren sind wichtige Konzepte in der organischen Chemie. Die verschiedenen Anordnungen und damit verbundenen Eigenschaften von Isomeren machen sie zu wertvollen Werkzeugen für die Entwicklung neuer Medikamente und Materialien. Moderne Techniken wie die NMR-Spektroskopie erlauben es, die genaue Molekülstruktur zu bestimmen und somit die spezifischen Eigenschaften einzelner Isomere zu analysieren.
Durch raffinierte Reaktionsmechanismen und Synthesemethoden gelingt es Wissenschaftlern, gezielt bestimmte Isomere herzustellen. Auf diese Weise können sie die gewünschten Eigenschaften für spezifische Anwendungen maximieren.
| Eigenschaft | Strukturisomere | Stereoisomere |
|---|---|---|
| Konnektivität der Atome | Unterschiedlich | Gleich |
| Räumliche Anordnung | Variabel | Unterscheiden sich |
| Beispiel für Bedeutung | Butan vs. Isobutan | Enantiomere in der Chiralität |
Identifikation und Analyse von Isomeren
Die Identifikation und Analyse von Isomeren ist ein zentraler Aspekt in der Chemie, um deren unterschiedliche chemische Eigenschaften und Reaktionsmechanismen zu verstehen. Verschiedene Techniken kommen hierbei zum Einsatz, die es ermöglichen, Strukturisomere sowie Stereoisomere präzise zu unterscheiden.
Eine übliche Methode zur Untersuchung der Molekülstruktur ist die Kernspinresonanz-Spektroskopie (NMR). Mit ihrer Hilfe kann die genaue Atomanordnung innerhalb eines Moleküls bestimmt werden. Insbesondere Konstitutionsisomere, bei denen die Verbindungen gleiche Summenformeln aber unterschiedliche Bindungsmuster haben, lassen sich dadurch gut identifizieren. NMR erlaubt es, Denkanstöße über die elektronische Umgebung einzelner Atome zu liefern und damit Rückschlüsse auf die chemischen Bindungen und funktionellen Gruppen zu ziehen.
Für stereochemische Untersuchungen, insbesondere zur Unterscheidung von enantiomeren und diastereomeren Molekülen, bietet sich die Verwendung der Röntgenkristallographie an. Diese Technik liefert detaillierte Informationen über die molekulare Symmetrie und die Kristallstruktur. Durch die exakte Vermessung des dreidimensionalen Aufbaus kann beispielsweise die Chiralität eines Moleküls ermittelt werden.
Auch chromatographische Methoden wie Hochleistungsflüssigkeitschromatographie (HPLC) spielen eine wichtige Rolle bei der Isomerentrennung. Hierbei wird die unterschiedliche Wechselwirkung von Isomeren mit einer stationären Phase genutzt, um diese voneinander zu trennen und individuell analysieren zu können. Das Zusammenspiel dieser verschiedenen Techniken ermöglicht es Wissenschaftlern, tiefgehende Einblicke in die Struktur und das Verhalten von Isomeren zu gewinnen.
Bedeutung in der Pharmakologie
Isomere spielen eine entscheidende Rolle in der Pharmakologie, da ihre chemischen und physikalischen Eigenschaften signifikant variieren können. Besonders wichtig ist dies bei Enantiomeren, welche Spiegelbilder voneinander sind. Diese spiegelbildlichen Moleküle können im menschlichen Körper unterschiedliche Wirkungen haben. Ein Beispiel dafür ist das Medikament Thalidomid: Während ein Enantiomer als Beruhigungsmittel fungiert, verursacht das andere schwerwiegende Missbildungen bei ungeborenen Kindern.
In vielen Arzneimitteln sind die gewünschten therapeutischen Effekte oft nur auf eines der möglichen Isomeren beschränkt. Daher ist es von größter Bedeutung, dass pharmakologische Studien präzise festlegen, welches Isomer die wirksame Substanz darstellt. Die Kenntnis über funktionelle Gruppen und deren Raumerfüllung innerhalb der Molekülstruktur hilft dabei, die chemischen Eigenschaften gezielt zu analysieren und geeignete Reaktionsmechanismen zu planen.
Zusätzlich ist die Trennung der Isomeren, auch bekannt als Isomerentrennung, erforderlich, um sicherzustellen, dass lediglich das wirksame Enantiomer verabreicht wird. Methoden wie NMR-Spektroskopie oder kristallstrukturelle Analysen unterstützen diese Prozesse erheblich. Die chemische Bindung und molekulare Symmetrie spielen hierbei eine wichtige Rolle zur Identifikation und Analyse verschiedener Isomere.
Somit beeinflussen Strukturisomere und Stereoisomere nicht nur die Synthese neuer Medikamente, sondern auch die Bewertung ihrer Sicherheit und Effektivität.
Umwandlung zwischen Isomeren
Die Umwandlung zwischen Isomeren, auch als Isomerisierung bekannt, ist ein spannender Bereich der Chemie. Diese Prozesse spielen eine wichtige Rolle in der organischen Chemie und betreffen sowohl Strukturisomere als auch Stereoisomere. Bei dieser chemischen Reaktion ändert sich die Anordnung der Atome im Molekül, ohne dass neue Bindungen gebildet oder alte gebrochen werden.
Ein konkretes Beispiel für die Umwandlung zwischen Strukturisomeren ist die Keto-Enol-Tautomerie. Hierbei verschieben sich das Proton und die Doppelbindung innerhalb eines Moleküls. Bei Stereoisomeren spielt insbesondere die thermische Isomerisierung von Cis-Trans-Isomeren eine große Rolle. Diese kann durch Einwirkung von Wärme oder Licht erfolgen, wobei es zu einer Rotation um eine Doppelbindung kommt.
Chirale Moleküle, die Enantiomere darstellen, können ebenfalls isomerisieren, jedoch sind besondere Katalysatoren notwendig, um das asymmetrische Zentrum des Moleküls zu verändern. Diese katalytische Racemisierung findet Anwendung in der Pharmakologie zur Herstellung enantiomerenreiner Verbindungen. Der Prozess wird oft durch Übergangsmetallkatalysatoren ermöglicht, die selektiv die Konfiguration eines chiralen Zentrums verändern können.
Zusammengefasst spielt die Kontrolle der Umwandlung zwischen Isomeren eine essentielle Rolle bei der gezielten Synthese bestimmter Verbindungen mit spezifischen chemischen Eigenschaften. Moderne Techniken wie NMR-Spektroskopie helfen dabei, diese Veränderungen in der Molekülstruktur genau zu verfolgen und zu analysieren.