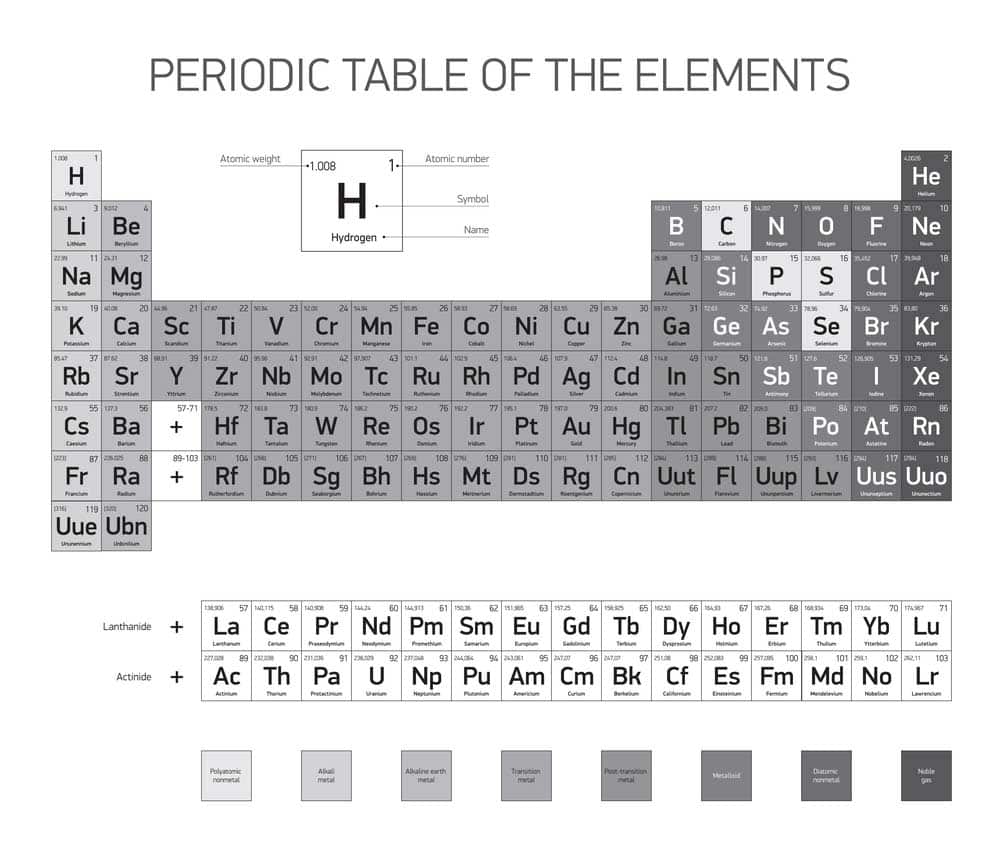
Das Periodensystem der Elemente ist ein grundlegendes Werkzeug in der Chemie. Es enthält alle bekannten chemischen Elemente, geordnet nach ihren Atomnummern und chemischen Eigenschaften. Eine wichtige Struktur des Periodensystems sind die sieben Hauptperioden, die die Zeilen im Periodensystem darstellen. Die Position eines Elements innerhalb einer Periode zeigt die Anzahl der Elektronenschalen an, die von seinen Atomen verwendet werden. Trotz ihrer unterschiedlichen Eigenschaften gibt es innerhalb jeder Periode bestimmte Muster und Wiederholungen, welche das periodische Gesetz veranschaulichen.
Das Wichtigste in Kürze
- Das Periodensystem besteht aus sieben Hauptperioden, die die Elektronenschalenanzahl der Elemente angeben.
- Eigenschaften der Elemente variieren innerhalb einer Periode von Metallen zu Nichtmetallen.
- Mit jeder neuen Periode treten schwerere Elemente mit komplexeren Elektronenkonfigurationen auf.
- Das periodische Gesetz zeigt Wiederholungsmuster der Elementeigenschaften nach Atomnummer.
- Perioden sind von 1 bis 7 nummeriert, entsprechend ihrer Elektronenschalen.
Periodensystem hat sieben Hauptperioden
Das Periodensystem hat sieben Hauptperioden, die einen wichtigen Aspekt der chemischen Elemente darstellen. Jede dieser Perioden beschreibt eine horizontale Reihe im Periodensystem, wobei die Anzahl der Perioden einer unmittelbaren Beziehung zur Anzahl der Elektronenschalen der Elemente in dieser Periode steht.
Die erste Periode besteht nur aus zwei Elementen: Wasserstoff und Helium, während spätere Perioden zunehmend mehr Elemente enthalten. Zum Beispiel umfasst die zweite Periode acht Elemente von Lithium bis Neon. Die Tatsache, dass das Periodensystem sieben Hauptperioden hat, hilft dabei, eine systematische Anordnung der Elemente basierend auf ihren atomaren und elektronischen Eigenschaften zu schaffen.
Im Verlauf der Perioden ändern sich viele physikalische und chemische Eigenschaften der Elemente regelmäßig. Dies beinhaltet zum Beispiel den Übergang von Metallen zu Halbmetallen und Nichtmetallen. Darüber hinaus nimmt die Atomgröße innerhalb einer Periode von links nach rechts ab, da die Kernladung zunimmt und die Elektronen stärker angezogen werden.
Die Kenntnis dieser sieben Perioden ist unerlässlich für ein fundamentales Verständnis der Chemie und ermöglicht es Wissenschaftlern und Chemikern, Vorhersagen über das Verhalten und die Reaktivität verschiedener Elemente zu treffen. Dieses System fördert auch das Konzept des periodischen Gesetzes, welches besagt, dass die Eigenschaften der Elemente auf regelmäßige Weise variieren, wenn man sie nach steigender Ordnungszahl anordnet.
Die Elemente, wenn sie nach Atomgewicht geordnet sind, zeigen eine deutliche Periodizität ihrer Eigenschaften. – Dmitri Mendelejew
| Periode | Anzahl der Elemente |
|---|---|
| 1 | 2 |
| 2 | 8 |
| 3 | 8 |
| 4 | 18 |
| 5 | 18 |
| 6 | 32 |
| 7 | 32 |
Perioden bestimmen Anzahl der Elektronenschalen
Im Periodensystem sind die Elemente in sieben Hauptperioden angeordnet, wobei jede Periode eine bestimmte Anzahl von Elektronenschalen repräsentiert. Die Anzahl der Elektronenschalen eines Atoms stimmt mit der Nummer der Periode überein, in der sich das Element befindet. Beispielsweise haben Elemente der ersten Periode eine einzige Elektronenschale, während Elemente der zweiten Periode zwei Schalen besitzen.
Die Struktur der Elektronenschalen beeinflusst maßgeblich die Eigenschaften der jeweiligen Elemente. Elemente einer bestimmten Periode weisen daher charakteristische Gemeinsamkeiten auf, wie etwa ihre Reaktivität und Bindungseigenschaften. Diese Grundlage führt dazu, dass chemische Muster und Trends innerhalb des Periodensystems erkennbar werden.
Mit zunehmender Periode steigen auch die Anzahl der Protonen und Neutronen im Kern der Elemente, wodurch neue und schwerere Elemente entstehen. Dadurch können die Elektronen entsprechend den spezifischen Energieniveaus geordnet werden, was zur typischen Anordnung der Elemente im Periodensystem führt.
Diese Organisation ermöglicht es Wissenschaftlerinnen und Wissenschaftlern, die Eigenschaftsmuster und -trends vorherzusagen sowie neue Verbindungen und Materialien zu entwerfen. Das zugrunde liegende Konzept der Periodenstruktur ist somit ein entscheidendes Instrument für das Verständnis der Chemie und ihrer Anwendungen. Näheres, z.B. periodisches Gesetz liefert tiefere Einblicke in diese faszinierende Ordnung der Materie.
| Periode | Anzahl Elektronenschalen | Höchste Ordnungszahl |
|---|---|---|
| 1 | 1 | 2 |
| 2 | 2 | 10 |
| 3 | 3 | 18 |
| 4 | 4 | 36 |
| 5 | 5 | 54 |
| 6 | 6 | 86 |
| 7 | 7 | 118 |
Elemente in Perioden variieren in Eigenschaften
Im Periodensystem unterscheiden sich die Elemente innerhalb einer Periode erheblich in ihren Eigenschaften. Zu Beginn jeder Periode finden wir Metalle, die allgemein durch ihre gute elektrische Leitfähigkeit gekennzeichnet sind.
Während man sich entlang der Periode bewegt, nehmen metallische Charakteristika ab und nicht-metallische Eigenschaften treten hervor. So findet man auf der rechten Seite der Tabelle typischerweise Nichtmetalle wie Sauerstoff, Phosphor oder Schwefel.
Ein weiteres bemerkenswertes Merkmal ist die Veränderung des Atomradius. Der Atomradius nimmt von links nach rechts in einer Periode ab, da zusätzliche Elektronen stärker vom zunehmend positiven Kern angezogen werden. Dies beeinflusst auch die Ionisierungsenergie, die Energie, die erforderlich ist, um ein Elektron aus einem Atom zu entfernen. Sie steigt im Allgemeinen von links nach rechts an.
Chemische Reaktivität variiert ebenfalls drastisch. Während Alkalimetalle am Anfang der Periode sehr reaktiv sind und leicht mit Wasser reagieren, weisen Edelgase am Ende der Periode eine geringe Reaktivität auf.
Diese Variationen resultieren aus Änderungen der atomaren Struktur und laden dazu ein, das Verhalten von Elementen systematisch zu erforschen.
Neue Perioden mit schwereren Elementen
Im Periodensystem der Elemente folgt auf jede Periode eine neue, die mit schwereren Elementen beginnt. Dies liegt daran, dass die Atomkerne der Elemente zunehmend mehr Protonen und Neutronen beinhalten.
Mit jeder neuen Periode wird das Periodensystem um eine Zeile ergänzt. Die Anzahl der Elektronen, die die Atome in den äußeren Schalen haben, nimmt ebenfalls zu. Dadurch weisen die Elemente in neuen Perioden oft neue chemische Eigenschaften auf.
Neue Elemente werden entdeckt und erforscht, was zur Erweiterung des Periodensystems führt. Die Aufnahme neuer Elemente stellt sicher, dass wir ständig ein aktuelles und umfassendes Verständnis der Materialwelt beibehalten.
Das Muster, bei dem nach jeder vollendeten Periode schwerere Elemente hinzukommen, geht mit einer erhöhten Komplexität der elektronischen Konfigurationen einher. Dies wirkt sich wiederum auf reaktive und physikalische Eigenschaften der Elemente aus.
Der Fortschritt in Wissenschaft und Technologie ermöglicht es uns, immer tiefer in die Struktur der Materie einzudringen und weiterhin die natürlichen Gesetze zu erkunden. Jeder Abschnitt im Periodensystem erzählt somit nicht nur die Geschichte einzelner Elemente, sondern auch die Entwicklung der menschlichen Erkenntnis.
Periodisches Gesetz beschreibt Wiederholungsmuster
Innerhalb des Periodensystems zeigt das periodische Gesetz, dass sich die Eigenschaften der Elemente in regelmäßigen Abständen wiederholen. Diese Regelmäßigkeit ergibt sich aus dem Aufbau der Atome und ihrer Elektronenschalen.
Die Anordnung der Elemente in einer bestimmten Reihenfolge basiert auf ihren Atomnummern. Dadurch ist es möglich, Muster in den physikalischen und chemischen Eigenschaften der Elemente zu erkennen.
Betrachten Sie zum Beispiel die Alkali- und Erdalkalimetalle: Innerhalb einer Periode ändern sich ihre Eigenschaften stetig von links nach rechts. Wenn man jedoch in die nächste Periode übergeht, sieht man, dass ähnliche Elemente mit vergleichbaren Eigenschaften erneut auftreten.
Diese Wiederholung erklärt, warum Lithium (in der ersten Periode) und Natrium (in der zweiten Periode) so viele gemeinsame Merkmale teilen. Beide sind weich, reagieren heftig mit Wasser und bilden Alkalilösungen. Das eVideo law, beschreibt die grundlegenden Muster im Verhalten der chemischen Elemente genauestens.
Zusammengefasst veranschaulicht dieser Zusammenhang, wie das periodische System genutzt wird, um Vorhersagen über unbekannte oder noch nicht entdeckte Elemente zu treffen. Damit ist das periodische Gesetz eine Schlüsselkomponente bei der Erforschung neuer Materialien und Verbindungen in der Chemie.
Perioden nummeriert von 1 bis 7
Die Perioden im Periodensystem der Elemente sind von 1 bis 7 nummeriert. Diese Nummerierung ist nicht willkürlich, sondern basiert auf der Anzahl der Elektronenschalen, die ein Atom jedes Elements in der jeweiligen Periode besitzt.
Elemente in der ersten Periode haben nur eine Elektronenschale, während diejenigen in der siebten Periode sieben Schalen besitzen. Dieses Schema hilft dabei, die Eigenschaften und das Verhalten von Elementen zu erklären, da ähnliche Strukturen oft ähnliche chemische Eigenschaften bedingen.
Während man sich von der ersten zur siebten Periode bewegt, nimmt die Anzahl der Protonen und Neutronen im Kern sowie die Anzahl der Elektronen in den Schalen kontinuierlich zu. Dies führt zu einer Vielzahl spannender physikalischer und chemischer Phänomene.
Jedem neuen Atom, das entdeckt wird und dessen Eigenschaften gemessen werden können, wird eine bestimmte Stelle innerhalb dieser Periodenstruktur zugewiesen. Dies erleichtert auch die Vorhersage der Eigenschaften neuer oder bislang weniger erforschter Elemente.
Das Wissen um die Perioden ist grundlegend für das Verständnis des gesamten Periodensystems und erweist sich als äußerst nützlich in verschiedenen Bereichen der Chemie und Physik.