Biochemische Reaktionen und Stoffwechselvorgänge in biologischen Systemen
Chemische Reaktionen in biologischen SystemenChemische Reaktionen in biologischen Systemen sind fundamental für das Verständnis aller lebenden Organismen. Diese Reaktionen steuern nahezu alle Prozesse in Zellen und Geweben, von der Energiegewinnung bis zur Informationsweitergabe.
Enzyme spielen hierbei eine zentrale Rolle als Biokatalyse. Sie beschleunigen biochemische Reaktionen und ermöglichen spezifische Stoffwechselwege. Ein gutes Beispiel dafür ist die Zellatmung, bei der über Glykolyse, Zitronensäurezyklus und Atmungskette ATP gewonnen wird.
Ein weiteres Schlüsselbeispiel ist die Photosynthese, bei der Lichtenergie in chemische Energie umgesetzt wird. Hierbei gelangen Elektronen durch verschiedene Moleküle und erzeugen letztlich Zucker und Sauerstoff. Diese Prozesse umfassen komplexe Reaktive Zwischenprodukte und benötigen spezialisierte Enzyme.
Die DNA-Replikation veranschaulicht ebenfalls die Bedeutung chemischer Reaktionen: Sie umfasst precise Mechanismen und Enzym-Substrat-Komplex-Bildungen für die Genverdopplung. Darüber hinaus spielen Signaltransduktion und Proteinmodifikation eine wesentliche Rolle in der Kommunikation zwischen und innerhalb von Zellen.
Schließlich sollte man sich die verschiedenen Stoffwechselwege anschauen, sowohl anabolisch als auch katabolisch. Diese sind Teil eines riesigen Netzwerks, das weitgehend durch Allosterische Regulation und andere Kontrollmechanismen gesteuert wird. Dies verdeutlicht die unglaubliche Komplexität und Effizienz biochemischer Systeme im Leben.
Das Wichtigste in Kürze
- Enzyme als Biokatalysatoren beschleunigen biochemische Reaktionen und sind in Stoffwechselwegen unverzichtbar.
- Zellatmung umfasst Glykolyse, Zitronensäurezyklus und Atmungskette zur Energiegewinnung in Form von ATP.
- Photosynthese wandelt Lichtenergie in chemische Energie um, produziert Zucker und Sauerstoff.
- DNA-Replikation benötigt spezifische Enzyme für präzise und fehlerfreie Genverdopplung.
- Anabole und katabolische Stoffwechselwege sind für Aufbau und Abbau von Biomolekülen verantwortlich.
Chemische Reaktionen in biologischen Systemen sind Prozesse, bei denen Moleküle in lebenden Organismen miteinander interagieren und umgewandelt werden. Diese Reaktionen spielen eine entscheidende Rolle bei lebenswichtigen Funktionen wie Stoffwechsel, Energiegewinnung, Signalübertragung, Zellteilung und vielen anderen biologischen Prozessen. Chemische Reaktionen in biologischen Systemen werden von Enzymen katalysiert, die spezifisch auf bestimmte Substrate wirken und die Reaktionsgeschwindigkeiten erhöhen, um effiziente biochemische Abläufe zu ermöglichen.
Beispiele
- Die Hydrolyse von Nahrungsmitteln im Verdauungstrakt durch Enzyme wie Amylase, Protease und Lipase ist ein Beispiel für eine chemische Reaktion in einem biologischen System. Dabei werden komplexe Kohlenhydrate, Proteine und Fette in einfachere Moleküle wie Zucker, Aminosäuren und Fettsäuren umgewandelt, die vom Körper aufgenommen werden können.
- Die Photosynthese in Pflanzen ist ein weiteres Beispiel für eine chemische Reaktion in einem biologischen System. Dabei wandeln Chloroplasten mithilfe von Lichtenergie und Enzymen Kohlendioxid und Wasser in Glukose und Sauerstoff um.
- Die Atmung in Lebewesen ist ein weiteres Beispiel für chemische Reaktionen in biologischen Systemen. Dabei wird Sauerstoff durch Enzyme in den Zellen zur Energiegewinnung verwendet und Kohlendioxid als Abfallprodukt abgegeben.
- Die DNA-Replikation ist ein weiteres wichtiges Beispiel für chemische Reaktionen in biologischen Systemen. Dabei werden die Basenpaarungen der DNA-Moleküle durch Enzyme repliziert, um die genetische Information zu verdoppeln.
- Die Proteinbiosynthese, bei der die genetische Information in der DNA in Proteine umgesetzt wird, ist ein weiteres Beispiel für chemische Reaktionen in biologischen Systemen. Dabei werden Aminosäuren durch Ribosomen zu Proteinen verknüpft.
- Die Signalübertragung in Nervenzellen durch chemische Reaktionen an den Synapsen ist ein weiteres Beispiel für die Komplexität chemischer Prozesse in biologischen Systemen. Dabei werden Neurotransmitter freigesetzt, um Nervenimpulse zu übertragen.
Enzyme als Biokatalysatoren: Beschleunigung biochemischer Reaktionen
Chemische Reaktionen in biologischen Systemen laufen oft nicht von selbst oder nur sehr langsam ab. Hier kommen Enzyme ins Spiel, die als Biokatalysatoren fungieren und biochemische Reaktionen erheblich beschleunigen.
Enzyme sind Proteine, die eine hohe Spezifität für ihre Substrate aufweisen. Dies bedeutet, dass sie bestimmte Moleküle erkennen und binden können. Der Schlüssel dazu ist der Enzym-Substrat-Komplex, welcher durch spezifische Wechselwirkungen stabilisiert wird.
Die Effizienz dieser Prozesse basiert auf dem „Schlüssel-Schloss-Prinzip“, bei dem das Enzym (das Schloss) perfekt zu seinem Substrat (dem Schlüssel) passt. Innerhalb des Enzyms befinden sich sogenannte katalytische Zentren, welche die chemische Umwandlung ermöglichen. Diese Zentren bestehen aus Aminosäureresten, die reaktive Zwischenprodukte stabilisieren und so die Aktivierungsenergie der Reaktion herabsetzen.
Ein weiterer wichtiger Aspekt der Biokatalyse ist die Allosterische Regulation. Durch Bindung eines Effektor-Moleküls an eine Stelle des Enzyms, die nicht das aktive Zentrum ist, kann die Aktivität des Enzyms gesteuert werden.
Viele Enzyme arbeiten zudem in Multienzymkomplexen zusammen. Solche Komplexe ermöglichen es, mehrere aufeinanderfolgende Reaktionen effizienter abzuwickeln. In biosynthetischen Bahnen koordinieren diese Komplexe die Synthese komplexer Biomoleküle wie Proteine und Nukleinsäuren.
Zusammenfassend sind Enzyme unverzichtbare Werkzeuge in metabolischen Netzwerken und spielen eine zentrale Rolle bei der Proteinmodifikation und vielen anderen biochemischen Prozessen.
Enzyme sind die Werkzeuge, die die Lebenskraft in chemische Aktionen umsetzen. – Albrecht Kossel
| Begriff | Beschreibung |
|---|---|
| Biokatalyse | Beschleunigung biochemischer Reaktionen durch Enzyme |
| Reaktive Zwischenprodukte | Instabile Moleküle, die während chemischer Reaktionen entstehen |
| Enzym-Substrat-Komplex | Der Komplex, der sich bildet, wenn ein Enzym an sein Substrat bindet |
| Biomimetische Reaktionen | Chemische Reaktionen, die natürliche Prozesse nachahmen |
| Katalytische Zentren | Regionen im Enzym, wo die chemische Umwandlung stattfindet |
| Multienzymkomplexe | Gruppen von Enzymen, die zusammenarbeiten, um aufeinanderfolgende Reaktionen zu katalysieren |
| Biosynthetische Bahnen | Abfolgen von Reaktionen, die zur Synthese von Biomolekülen führen |
| Allosterische Regulation | Regulation der Enzymaktivität durch Bindung an eine andere Stelle als das aktive Zentrum |
| Metabolische Netzwerke | Verknüpfungen verschiedener Stoffwechselwege in einer Zelle |
| Proteinmodifikation | Veränderungen an Proteinen nach deren Synthese, z.B. Phosphorylierung |
Zellatmung: Energiegewinnung durch Glykolyse, Zitronensäurezyklus, Atmungskette
Die Zellatmung ist ein zentraler Prozess der Energiegewinnung in Zellen. Sie umfasst drei Hauptschritte: Glykolyse, Zitronensäurezyklus und die Atmungskette.
In der Glykolyse, welche im Zytoplasma stattfindet, wird Glukose in zwei Moleküle Pyruvat zerlegt. Dabei entstehen ATP und NADH als Energieprodukte. Der eigentliche Verbrauch von Sauerstoff beginnt jedoch erst nach der Glykolyse.
Im Zitronensäurezyklus, auch Krebs-Zyklus genannt, werden die Pyruvatmoleküle weiter abgebaut. Dieser Zyklus findet in den Mitochondrien statt und produziert zusätzliches ATP sowie Elektronen, die an Coenzyme wie NADH und FADH2 gebunden werden. Diese Coenzyme spielen eine entscheidende Rolle bei der Übertragung von Elektronen zur nächsten Stufe.
Die letzte Phase ist die Atmungskette oder oxidative Phosphorylierung, die ebenfalls in den Mitochondrien lokalisiert ist. Hier werden die Elektronen von NADH und FADH2 durch eine Reihe von Proteinkomplexen transferiert. Die finale Elektronenakzeptanz erfolgt durch Sauerstoff, was zur Bildung von Wasser führt. Während dieses Prozesses wird ein Protonengradient aufgebaut, der letztlich genutzt wird, um großen Mengen an ATP zu synthetisieren.
Durch diese Schritte wird deutlich, dass die Zellatmung nicht nur einfach chemische Reaktionen sind, sondern komplexe, integrierte Prozesse, die auf spezifischen Enzymen beruhen. Jeder Schritt weist charakteristische Katalytische Zentren auf, die spezifisch für bestimmte Substrate und Reaktionen ausgelegt sind.
Photosynthese: Lichtenergie in chemische Energie umwandeln
Chemische Reaktionen in biologischen Systemen spielen eine zentrale Rolle bei der Photosynthese. In diesem Prozess wird Lichtenergie genutzt, um sie in chemische Energie umzuwandeln. Diese Energieumwandlung erfolgt hauptsächlich in den Chloroplasten von Pflanzenzellen.
Bei der Photosynthese wird Lichtenergie durch die Absorption von Photonen durch Chlorophyllmoleküle eingefangen. Diese angeregten Elektronen werden durch eine Reihe von Elektronentransferkomplexen geleitet, was zur Bildung eines Protonengradienten führt. Der erzeugte Protonengradient treibt das Enzym ATP-Synthase an, das ADP in ATP umwandelt – die Energiespeichermoleküle der Zelle.
Ein weiterer wichtiger Bestandteil der Photosynthese ist die Fixierung von Kohlendioxid. Im Calvin-Zyklus, einer Serie von chemischen Reaktionen, wird Kohlendioxid mit Hilfe des Enzyms RuBisCO in organische Moleküle eingebaut. Diese Moleküle werden anschließend zu Glukose und anderen Kohlenhydraten verarbeitet, welche als Hauptnahrungsquelle für die Pflanze dienen.
Reaktive Zwischenprodukte wie NADPH spielen ebenfalls eine entscheidende Rolle im Calvin-Zyklus, indem sie die notwendigen Reduktionsäquivalente liefern. Diese biochemischen Prozesse zeigen die Komplexität und Effizienz biologischer Systeme bei der Umwandlung und Speicherung von Energie.
Durch die Erforschung dieser biomimetischen Reaktionen könnten zukünftig neue Wege gefunden werden, um Sonnenenergie effizienter zu nutzen. Die Untersuchung der jeweiligen katalytischen Zentren und Multienzymkomplexe liefert wertvolle Einblicke in die Natur dieses essenziellen biologischen Prozesses.
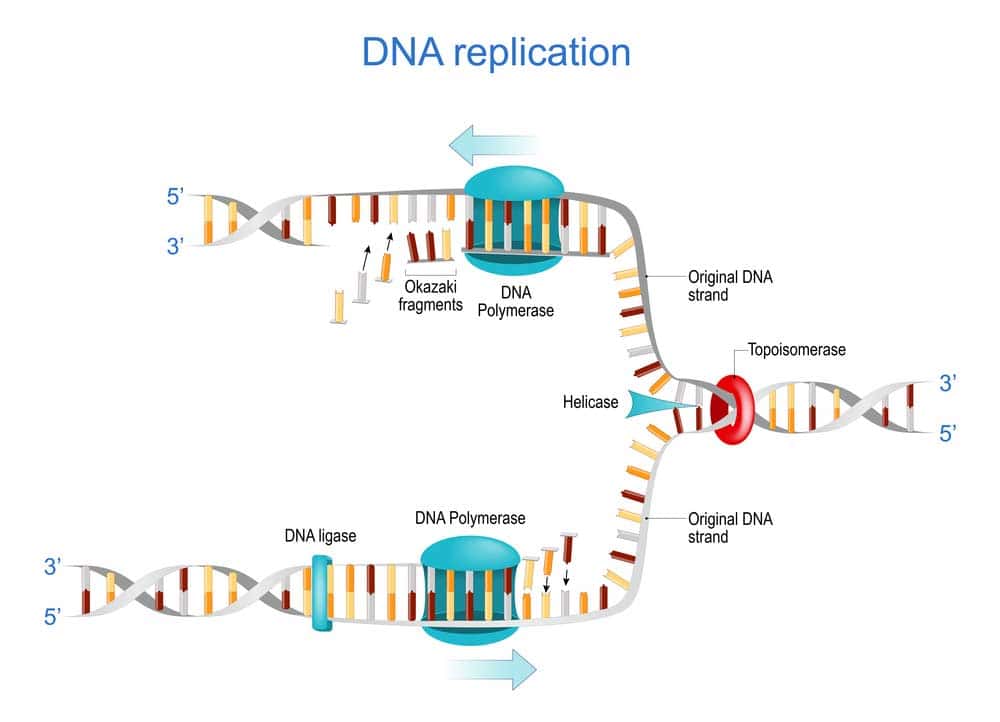
DNA-Replikation: Mechanismen und Enzymprozesse der Genverdopplung
Die DNA-Replikation ist ein wesentlicher Prozess in biologischen Systemen, der sicherstellt, dass genetische Informationen genau verdoppelt werden. Während dieses Prozesses arbeiten zahlreiche Enzyme zusammen, um die DNA-Doppelhelix zu entspannen, aufzubrechen und neue Stränge zu synthetisieren.
Zu Beginn entwindet das Enzym Helikase die Doppelhelix und trennt die beiden DNA-Stränge voneinander, wodurch eine Replikationsgabel entsteht. Danach bindet die Primase kurze RNA-Primer an die einzelnen Stränge, die als Startpunkt für die DNA-Synthese dienen.
Die bedeutendste Rolle spielt die DNA-Polymerase, die neue Nukleotide basierend auf dem Matrizenstrang hinzufügt und so den neuen komplementären Strang bildet. Dabei entstehen zwei identische Doppelhelixe aus einem Ursprungsmolekül. Dieser Vorgang enthält zusätzliche Sicherheitsmechanismen, wie die Korrekturlesefunktion der DNA-Polymerase, um Fehler während der Synthese zu minimieren.
Außerdem sind mehrere Enzyme beteiligt, die Reaktive Zwischenprodukte handhaben oder den Prozess stabilisieren, darunter Ligase, die Okazaki-Fragmente im Folgestrang verbindet, und Topoisomerase, die Überspiralisierungen der DNA verhindert.
Letztlich ermöglicht die komplexe Zusammenarbeit dieser Enzyme einen präzisen und effizienten Nachbau des Erbguts, grundlegend für Zellteilung und Vererbung. Hierbei spielen Katalytische Zentren und allosterische Regulation eine Schlüsselrolle in der Effizienz und Genauigkeit des Prozesses.
Signaltransduktion: Zellkommunikation durch chemische Signalstoffe
Signaltransduktion ist der Prozess, durch den Zellen chemische Signale empfangen und weiterverarbeiten. Diese Signale stammen oft von anderen Zellen oder aus der Umgebung der Zelle selbst.
Chemische Signalstoffe wie Hormone oder Neurotransmitter binden an spezialisierte Rezeptoren auf der Zelloberfläche. Dieser Bindungsvorgang löst eine Kaskade von intrazellulären Ereignissen aus, die schließlich zu einer spezifischen zellulären Antwort führen. Ein häufiges Beispiel hierfür sind G-Protein-gekoppelte Rezeptoren, die nach Aktivierung das angekoppelte G-Protein aktivieren und dadurch weitere Signale innerhalb der Zelle verteilen.
Die Bedeutung der Signaltransduktion liegt in ihrer Fähigkeit, spezifische und koordinierte Antworten auf externe Stimuli zu ermöglichen. So können Zellen auf Veränderungen in ihrer Umgebung reagieren und Prozesse wie Zellwachstum, Differenzierung oder Apoptose (programmierten Zelltod) regulieren.
Ein zentraler Aspekt dieses Prozesses ist die Bildung von Enzym-Substrat-Komplexen, die die Signalübertragung verstärken und modulieren. Hierbei spielen auch biomimetische Reaktionen eine Rolle, bei denen künstlich erzeugte Reaktionen natürliche biologischen Prozessen nachempfunden sind, um deren Mechanismen besser zu verstehen und zu nutzen.
Allosterische Regulation und Proteinmodifikation sind ebenfalls wichtige Werkzeuge in der Signaltransduktion. Durch die Modifizierung von Proteinen können Signalketten ein- oder ausgeschaltet werden, was zur Feinabstimmung der zellulären Reaktionen beiträgt.
| Prozess | Reaktion | Beschreibung |
|---|---|---|
| Zellatmung | Glykolyse | Abbau von Glukose zu Pyruvat |
| Photosynthese | Calvin-Zyklus | Umwandlung von CO₂ in organische Moleküle |
| DNA-Replikation | Helikase Aktivität | Entwindung der DNA-Doppelhelix |
Metabolismus: Anabolische und katabolische Stoffwechselwege
Chemische Reaktionen in biologischen Systemen sind eng mit dem Metabolismus verbunden. Der Metabolismus kann in zwei grundlegende Prozesse unterteilt werden: anabolische und katabolische Stoffwechselwege.
Anabole Stoffwechselwege sind für den Aufbau komplexer Moleküle aus einfacheren Vorstufen verantwortlich. Diese Prozesse erfordern Energie, die häufig in Form von ATP bereitgestellt wird. Typische Beispiele für anabole Reaktionen sind die Proteinsynthese und die DNA-Replikation, bei denen Aminosäuren zu Proteinen und Nukleotide zu DNA-Strängen zusammengefügt werden.
Auf der anderen Seite stehen katabolische Stoffwechselwege, die den Abbau komplexer Moleküle zu einfacheren Verbindungen beinhalten. Dieser Prozess setzt chemische Energie frei, die dann vom Organismus genutzt werden kann. Ein klassisches Beispiel ist die Zellatmung, bei der Glukose abgebaut wird und dabei Energie freigesetzt wird.
Eine wichtige Rolle spielen auch Enzyme als Biokatalysatoren bei diesen Prozessen. Sie ermöglichen eine effiziente Steuerung und Regulation, ohne selbst verbraucht zu werden.
In beiden Fällen entstehen reaktive Zwischenprodukte, die weiterverarbeitet oder reguliert werden müssen. Multienzymkomplexe und katalytische Zentren innerhalb der Zelle steuern diese Abläufe präzise. Die allosterische Regulation trägt ebenfalls dazu bei, dass die verschiedenen Biosynthetischen Bahnen und metabolischen Netzwerke flexibel auf die Bedürfnisse der Zelle reagieren können.
Zusammenfassend ermöglichen diese Stoffwechselwege den Organismen nicht nur, Energie bereitzustellen und Biomoleküle aufzubauen, sondern sie sind auch ein Schlüsselelement für das Funktionieren lebender Systeme.
Proteinsynthese: Transkription und Translation in Zellen
Die Proteinsynthese ist ein zentraler Prozess in lebenden Zellen, der aus zwei Hauptschritten besteht: Transkription und Translation.
In der Transkription wird die genetische Information der DNA in eine mRNA umgeschrieben. Dies geschieht im Zellkern, wo das Enzym RNA-Polymerase an die DNA bindet und einen spezifischen Abschnitt, das Gen, abliest. Nachdem die mRNA synthetisiert wurde, verlässt sie den Zellkern und wandert ins Zytoplasma zur Ribosomen für den nächsten Schritt.
Im Ribosom, einem Komplex aus Proteinen und rRNA, findet die Translation statt. Hier wird die Basensequenz der mRNA in eine Aminosäuresequenz übersetzt, die dann zu einem funktionellen Protein gefaltet wird. Transfer-RNAs (tRNAs) transportieren dabei die passenden Aminosäuren entsprechend den Codons auf der mRNA zum Ribosom. Die tRNA besitzt spezielle Anticodons, die komplementär zu den mRNA-Codons sind und somit sicherstellen, dass die richtige Aminosäure eingebaut wird.
Beide Prozesse, sowohl Transkription als auch Translation, unterliegen einer strengen Kontrolle durch die Zellmaschinerie. Allosterische Regulation kann die Aktivität von Schlüsselenzymen modulieren, während Proteinmodifikationen nach der Synthese die Funktionalität und Lebensdauer der Proteine beeinflussen. Im Kontext der chemischen Reaktionen in biologischen Systemen spielen diese Mechanismen eine zentrale Rolle, da sie die Effizienz und Zuverlässigkeit der Proteinsynthese gewährleisten.
Der gesamte Prozess der Proteinsynthese zeigt, wie Biokatalyse und multienzymatische Systeme zusammenarbeiten. Jede Stufe ist präzise orchestriert, um sicherzustellen, dass die Zelle die benötigten Proteine effizient und fehlerfrei produziert.
Redoxreaktionen: Elektronentransferprozesse in biologischen Systemen
Redoxreaktionen spielen eine zentrale Rolle in biologischen Systemen. Sie beinhalten den Transfer von Elektronen zwischen Molekülen, was zu Veränderungen in ihrer Oxidationsstufe führt. Diese Prozesse sind für viele lebenswichtige Funktionen unerlässlich.
In der Zellatmung etwa werden Redoxreaktionen zur Energiegewinnung genutzt. Während der Glykolyse und des Zitronensäurezyklus treten Zwischenprodukte auf, die Elektronen auf spezialisierte Carrier-Moleküle übertragen. Diese Elektronen werden letztlich durch die Atmungskette weitergeleitet, wodurch ein Protonengradient geschaffen wird, der für die ATP-Synthese notwendig ist.
Auch bei der Photosynthese spielen Redoxreaktionen eine entscheidende Rolle. Hier werden Elektronen von Wasser abgespalten und durch verschiedene Trägermoleküle transportiert, um NADPH zu bilden und ATP zu synthetisieren. Diese Moleküle dienen dann als Energiequelle für die Fixierung von Kohlendioxid in Zucker.
Eine besondere Bedeutung haben auch enzymatische Redoxreaktionen, bei denen Enzyme als Biokatalysatoren fungieren. Dazu gehören beispielsweise Cytochrome, die im Rahmen ihres katalytischen Zyklus Elektronen aufnehmen und abgeben. Genau wie andere Enzyme wirken sie durch Bildung eines spezifischen Enzym-Substrat-Komplexes an ihren katalytischen Zentren.
Darüber hinaus sind wasserstofftransfernde Enzyme wie Dehydrogenasen wichtig, die durch Elektronentransfer ihre Substrate oxidieren oder reduzieren. Diese enzymatischen Prozesse können komplex sein und oft mehrere Stufen umfassen, einschließlich Zwischenprodukten und allosterischer Regulation. Insgesamt verknüpfen diese Reaktionen verschiedenste Stoffwechselwege und tragen zur Aufrechterhaltung funktioneller Metabolische Netzwerke bei.